粘膜下層剥離術 (ESD)
粘膜下層剥離術 (ESD) とは
当院では大腸粘膜下層剥離術 (ESD:Endoscopic Submucosal Dissection) を行っています。
大腸粘膜下層剥離術とは大腸の早期がんや腺腫などに対する内視鏡治療の一つで、病変の下の粘膜下層まで含めて一括で切除する手術です。
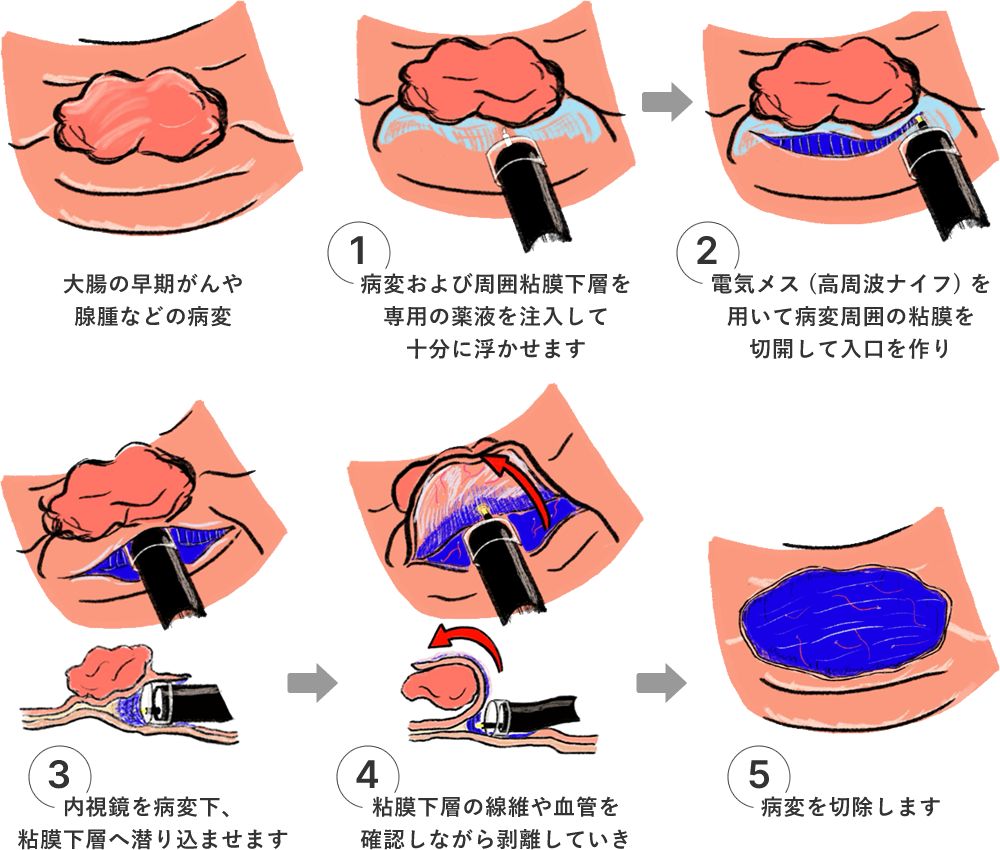
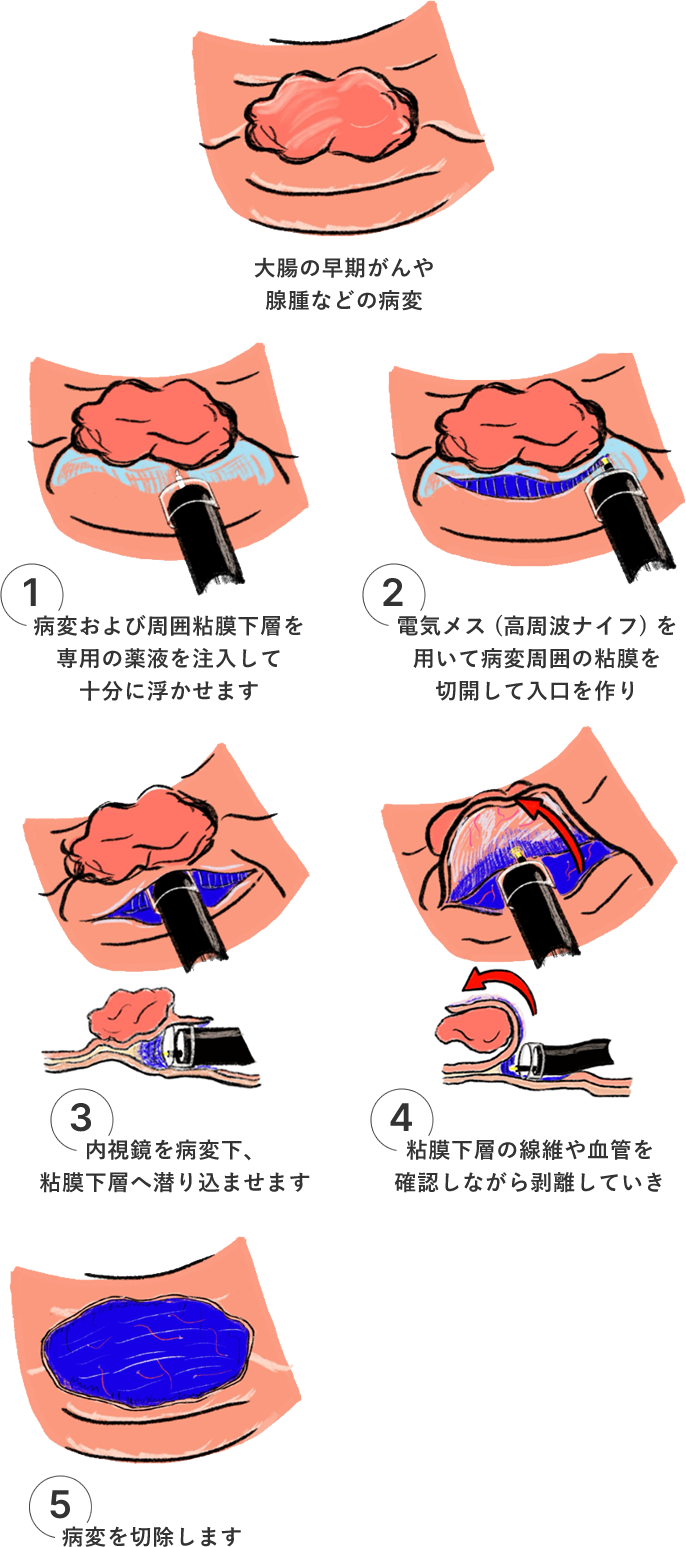
まず病変および周囲粘膜下層を専用の薬液を注入して十分に浮かせます (図1)。電気メス (高周波ナイフ) を用いて病変周囲の粘膜を切開して入口を作り (図2)、内視鏡を病変下 粘膜下層へ潜り込ませます (図3)。粘膜下層の線維や血管を確認しながら剥離していき病変を切除します (図4図5)。
従来の治療法では難しかった大きな病変も一括で切除でき、病理診断の精度向上や臓器温存による患者さんの負担軽減が期待できます。
当院で大腸ESDを行う理由
当院で大腸ESDを行う理由は2つあります。
理由その1. 病変をきれいに切り取るため
まずきっかけとなったのは『従来の方法 (ポリペクトミーやEMR) では綺麗に取りきれない病変に出くわす』こと。
例えば2cmを超える比較的大きな腫瘍にポリペクトミーあるいはEMRなどの従来の方法でスネアをかけても、腫瘍の背側にマージン (断端の余剰分) をとって十分にかけられているかどうかは視認できません。
えいっ、やっ、と勘や手探りでスネアをかけて通電切除しても、実際は腫瘍背側にひっかかっていると、腫瘍がぶつ切りになってしまいます。
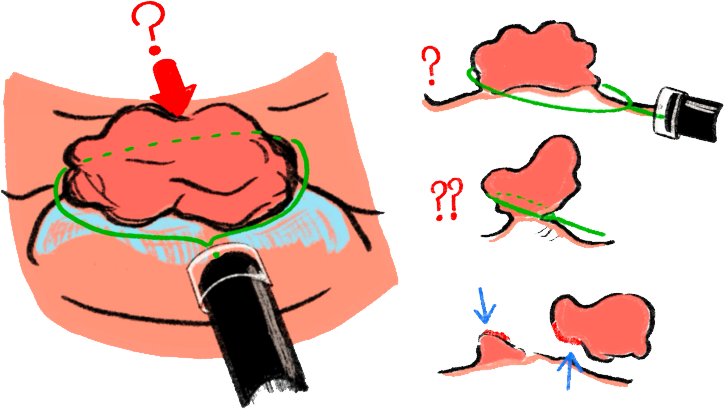
ぶつ切りで綺麗に切除できない場合 (追加で遺残した腫瘍を技術的には切除できますが)、その切除標本では切除腫瘍自身に熱変性が加わったりして精密な病理検査に支障を来たします。
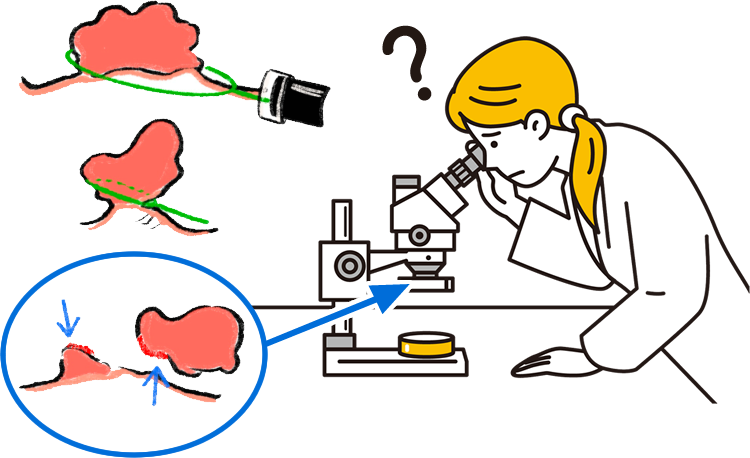
病理検査に支障が出ると、その後の患者さんの治療方針に大きな迷いが生じてしまいます。
内視鏡切除で根治できているかどうか追加の手術が必要かどうかを判断するには、病理学的に深達度は何ミクロンの深さか?リンパ管や血管など脈管侵襲はないか?断端に遺残はないか?など精密な検索に耐えうる切除標本である事が最低条件です。
見た目だけでなく綺麗に取れたかどうかは、逆に言えば綺麗にとれていないと病理検査の精度を著しく損い、引いては患者さんに不利益をもたらしてしまう結果となるのです。
きっかけとなった手痛い症例を動画で供覧いたします。
40mmと大きなIsp polypでした。幸いにして粘膜内癌で内視鏡的根治、その後のフォローでも再発は認めていませんが、この症例を経て従来のスネアでの切除では、まさに「先が見えない」「進歩がない」と痛感するとともに、真剣にESDに取り組もうと決意した一例でした。
理由その2. 住み慣れた地域での治療完結を
もう一つ当院で大腸ESDを行う理由は、当院のミッションとして『住み慣れた地域で完結できる診療』を掲げています。堅苦しい言葉で言うと、医療レベルの地域格差是正です。
大きい病院の多い都会で生まれ暮らしていたら長時間かけて通院せずに治療できるのに…とか (付き添いのご家族を含め)、地域の方々に損をさせたくない思いがあります。
島原半島内で大腸ESDに取り組んでいるのは当院だけです。(当方調べ)
リスクの高い手技ですので、細心の注意を払い最善を尽くせるよう心がけております。
ハイボリュームセンターでの研修など最前線ハイレベルの治療を吸収し、日々研鑽して地域の皆様に還元、貢献できるよう邁進してまいります。
今後、当院で行なったESDに関して随時発信してまいります。
2025(R7).9/21記
大腸ESD 2症例目
2例目は、前回1例目と似た、頭 (病巣) が大きく、茎 (頚部) が幅広で短いIsp polypです。前回は見えない部位 (特に腫瘍背側) を勘や手探りでイメージしながらスネアリングを試みましたが、病巣がぶつ切りになり一括切除できず惨憺たる結果でした。スネアリング手技のみでは限界を痛感しました。同じ轍を踏まないように今回はESDでの切除を試みました。
本症例のポイントは
①豊富な血流:茎の中を走行している太い栄養血管(動脈)、ドレナージ静脈の処理
②確実なマージン確保
③呼吸性変動:視野確保難、スコープの操作性難
などが挙げられます。(↓こちらの動画内でも言及しています)
やはりESDは手技としては高難易度ですが、病巣とマージンを視認しながらコツコツと切除できる利点は絶大で、その積み重ねで一括切除が可能でした。
まだまだ反省点や改善点は多々ありますが、前回1例目のリベンジ?をある程度果たせたか、、、あるいは回答をある程度出せたかと思います。
2026(R8).2/1記
大腸ESD 3症例目
大腸ESD治療のそもそもの始まりは、1例目や2例目のような頭 (病巣) の大きいIpやIspポリープからではありません。これらはあくまで派生です。
もともとはある割合で現れる大腸LST (側方発育型腫瘍) に対しての治療から始まりました。
下図のように横幅の広い腫瘍です。
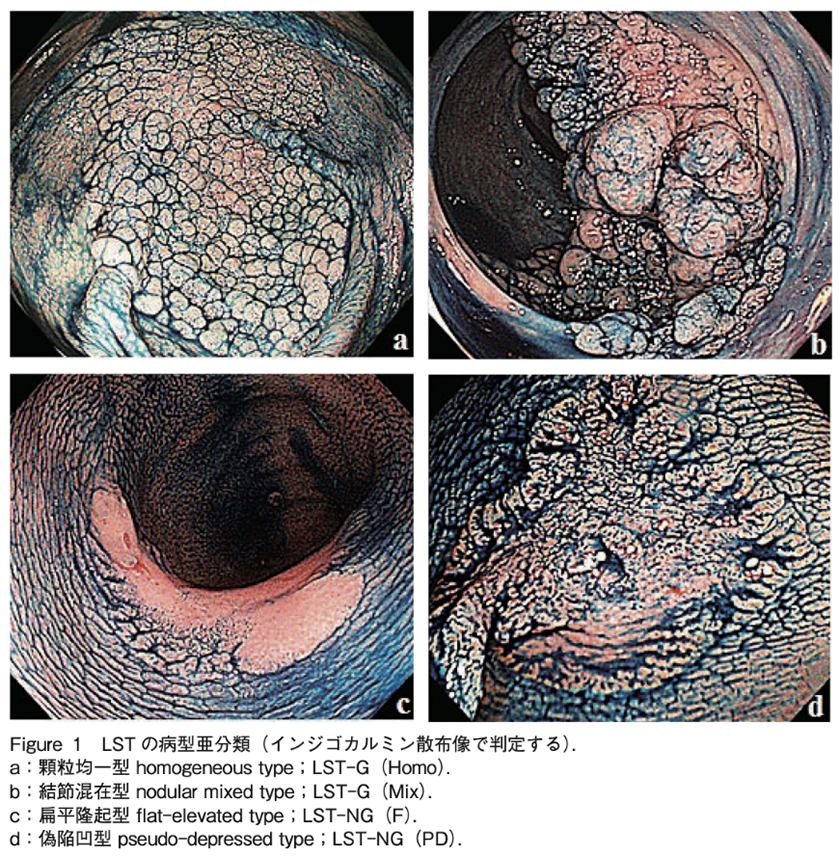
大腸ESD/EMRガイドライン(第2版)より
大腸LST(側方発育型腫瘍)の発見頻度は
昭和大学横浜市北部病院消化器センターで治療された腺腫からpT1癌の10.5%
ESDの適応となる大腸腫瘍(腺腫、早期癌)は内視鏡的治療適応病変の10%ほど(5mm以下の微小ポリープを除く)と言われています。
大腸LSTは従来のポリペクトミースネアでの切除ではひとまとめの切除(一括切除)が困難な病変です。
スネアの剛性(変形のしにくさ)や滑りなどの為、一括切除が困難となる事が多くなります。
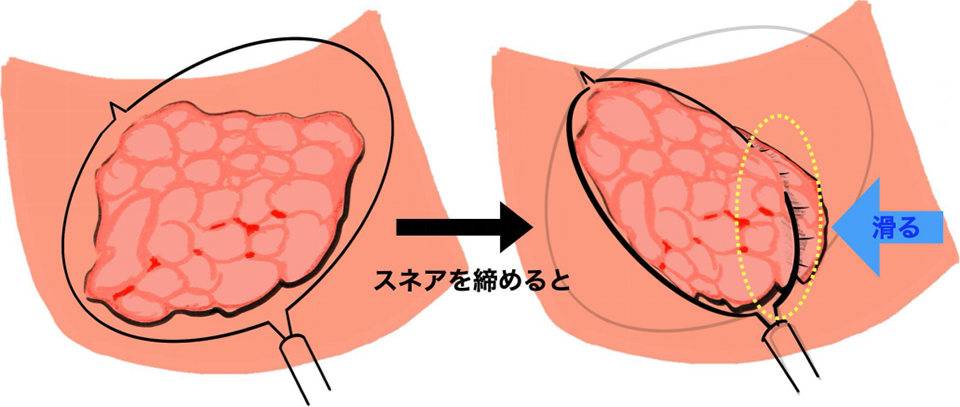
スネアで一括切除ができるのは平均2cmの大きさまでです。
以前はスネアによる分割切除あるいは外科手術による腸切除などが行われていました。
分割切除の場合、1回目の投稿でご説明したとおり病理学的検索が難しくなったり、病気が残ってしまう可能性があります(不完全切除)。
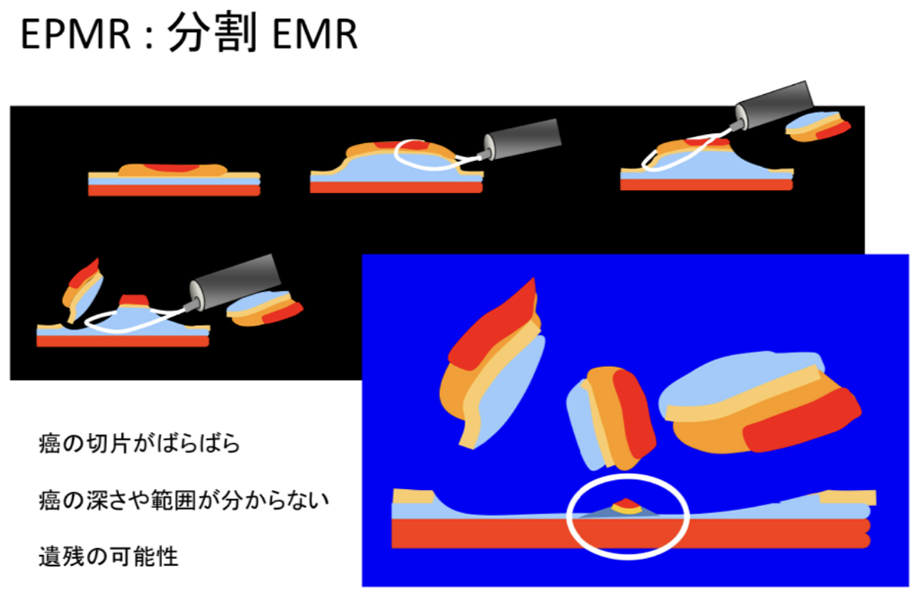
引用のシェーマです
外科手術腸切除は、多目に見積もっても早期癌の病変に対して患者さんへの侵襲が過大となってしまいます。
このような問題点を解決するために大腸病変に対してもESDが行われるようになりました。
今回はオーソドックスな大腸ESDの2例をご紹介いたします。
文責:土井 康郎 2026(R8).2/19記

電話受付時間
平日 9:00~17:00 / 土曜 9:00~14:30